Potássio baixo em gatos

Image by Flickr.com, courtesy of Enrico
Os baixos níveis de potássio em gatos é relativamente fácil de tratar, mas pode ser uma indicação de um problema mais sério de saúde. De acordo com o site "Petplace.com", alguns gatos com baixa de potássio podem ter problemas durante a vida toda.
Definição

Image by Flickr.com, courtesy of Pop!Tech
O baixo nível de potássio em gatos é conhecido como hipocalemia felina. Os sintomas não são restritos para essa doença.
Sinais e sintomas

Image by Flickr.com, courtesy of Judi Cox
Os gatos com hipocalemia podem parecer cansados, fracos, duros e cessarem os movimentos normais do intestino. Eles possuem sede constante e urinam muito também.
Causas
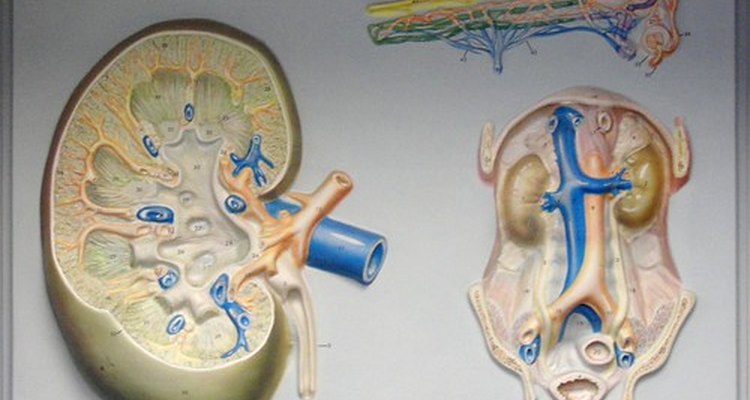
Image by Flickr.com, courtesy of hobvias sudoneighm
A causa mais comum de hipocalemia em gatos é a insuficiência renal crônica; a diabetes felina é outra causa potencial. É possível que alguns gatos birmaneses herdem baixas de potássio, de acordo com o autor Cheryl L. Chrisman.
Diagnóstico
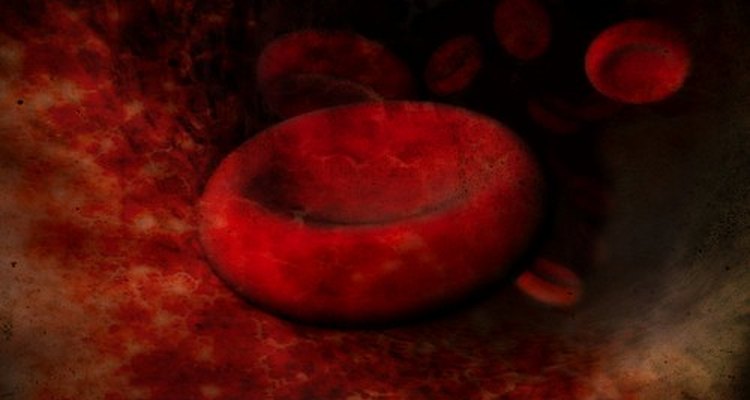
Image by Flickr.com, courtesy of Andrew Mason
Os veterinários detectam a hipocalemia, testando o sangue do gato e fazendo exames no coração, já que essa condição afeta a função cardiovascular de um gato. Os gatos com insuficiência renal podem mostrar baixa de glóbulos vermelhos, causando anemia.
Tratamento

Image by Flickr.com, courtesy of Vittorio Vittori
A hipocalemia felina pode levar à hospitalização. Normalmente, os veterinários prescrevem um líquido, o suplemento de potássio pastoso (gluconato de potássio), que também é dado para tratar essa doença.
Prevenção/Solução

Image by Flickr.com, courtesy of Ma1974
Impeça a hipocalemia felina com comida de gato de qualidade. Use suplementos necessários e que foram prescritos.
Referências
Sobre o Autor
Josalin Mitchell began her writing career in 2009. She has written web content as well as grants, training manuals, reports and brochures for nonprofit agencies. Mitchell has a Bachelor of Arts in English and women's studies and is currently pursuing a Master of Arts in Teaching in English education.
Créditos Fotográficos
Image by Flickr.com, courtesy of Enrico






