Como calcular átomos para mols para gramas
Hemera Technologies/PhotoObjects.net/Getty Images
Na química, um mol representa um grande número de átomos, moléculas ou outras partículas microscópicas. No caso de converter de átomos para mols, um mol contém 6,022 x 10^23 átomos. Os mols também têm outra propriedade útil: um mol de qualquer substância tem a massa em gramas igual ao peso molecular da substância. Armado com o conhecimento das propriedades do mol e uma tabela periódica, você pode converter átomos para moléculas para gramas de qualquer substância.
Step 1
Divida o número de átomos pelo número de Avogadro, 6,022 x 10^23, para achar o número de mols. Se você tem 5 x 10^24 átomos de nitrogênio, por exemplo, divida-o por 6,022 x 10^23 para obter 8,3 mols de nitrogênio.
Step 2
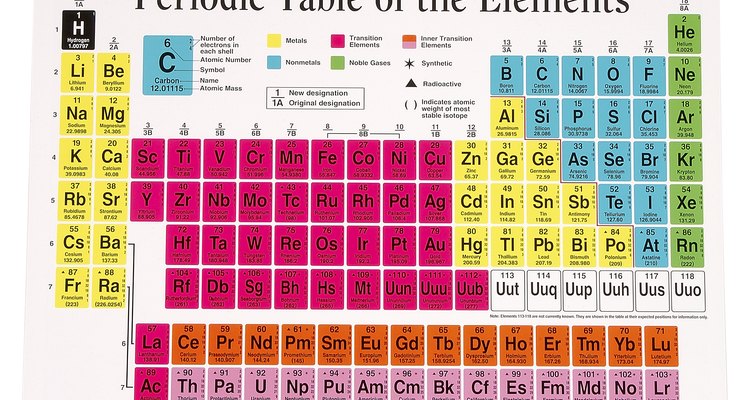
Procure pelo elemento da tabela periódica e verifique o número embaixo do símbolo do elemento em gramas por mol para obter o peso molecular. O símbolo para o nitrogênio é N, por exemplo, e o número embaixo do N na tabela periódica é 14,0067, então o peso molecular do nitrogênio é 14,0067 g/mol.
Step 3
Multiplique o peso molecular pelo número de mols para obter a massa. Para 8,3 mols de nitrogênio, multiplique-o por 14,0067 g/mol para obter 116,26 g de nitrogênio.
Mais Artigos
Como converter gramas para a concentração de mol/L→

Como descobrir o percentual de erro ao calcular a densidade→

Como calcular o fator de empacotamento do diamante cristalino→

Como inserir o símbolo cúbico→

Alimentos ricos em citrato de potássio→

Como calcular a concentração percentual de sulfato de cobre no sulfato de cobre penta-hidratado →

Referências
Dica
- O mesmo procedimento funciona para conversão entre moléculas, mols e gramas-- apenas tenha certeza de adicionar o peso molecular de todos os átomos da molécula antes de multiplicar pelo número de mols.
Advertência
- Certifique-se de ler o peso molecular ao invés do número atômico na tabela periódica. O peso molecular geralmente fica abaixo do símbolo do elemento, e o número atômico fica acima. Você pode confirmar olhando se o seu número tem casas decimais; os números atômicos são sempre inteiros.
Sobre o Autor
Petra Wakefield is a writing professional whose work appears on various websites, focusing primarily on topics about science, fitness and outdoor activities. She holds a Master of Science in agricultural engineering from Texas A&M University.
Créditos Fotográficos
Hemera Technologies/PhotoObjects.net/Getty Images
